
Stöchiometrie – Schritt für Schritt erklärt
Beim Rechnen in der Chemie ist das Aufstellen und Umformen von Formeln eine der wichtigsten Grundlagen. Auf dieser Seite lernst du Schritt für Schritt, wie du chemische Formeln sicher anwendest – mit Beispielen, Merkhilfen und Übungen.Weiterführende Themen aus dem Bereich der 8. Klasse – Überblick
- Endo- & Exotherme Reaktionen
- Benennung binärer Verbindungen
- Reaktionsgleichungen lösen
Hauptvideo Formeln aufstellen & umformen
Das Aufstellen und Umformen von Formeln gehört zu den wichtigsten Grundlagen der quantitativen Chemie. Egal ob du die Dichte, die Stoffmenge oder das Volumen berechnen möchtest – mit den richtigen 3-4 Formeln kannst du viele Aufgaben der 8. Klasse sicher lösen.
Auf dieser Seite lernst du Schritt für Schritt, wie du Formeln aufstellst, umformst und in Rechenaufgaben anwendest.
Das Video zu den Rechenaufgaben gliedert sich in folgende Schritte:
- Aufstellen
- Umformen
- Merkhilfen
- Rechenbeispiel
Grundlagen Rechnen – Berechnung der Dichte
Einige Rechenaufgaben aus der Chemie setzen zusätzlich die Kenntnis zur Berechnung der Dichte voraus. Dies ist insbesondere der Fall, wenn es um Berechnungen mit Volumina von Flüssigkeiten geht. Bei Volumen denkt man sofort an das molare Volumen. Hierbei muss aber berücksichtigt werden, dass Berechnungen mit dem molaren Volumen ausschließlich mit Gasen stattfinden dürfen. Bei Volumina von Flüssigkeiten muss man über die Dichte weiterarbeiten und damit die Masse berechnen.Formeln aufstellen Chemie – einfach erklärt
Beim Rechnen in der Chemie musst du häufig Formeln umstellen, um eine gesuchte Größe zu berechnen – zum Beispiel die Stoffmenge, die Masse oder das Volumen. Damit das zuverlässig klappt, gibt es eine einfache Methode, die dir das Leben deutlich leichter macht: das Umformungs‑Dreieck.
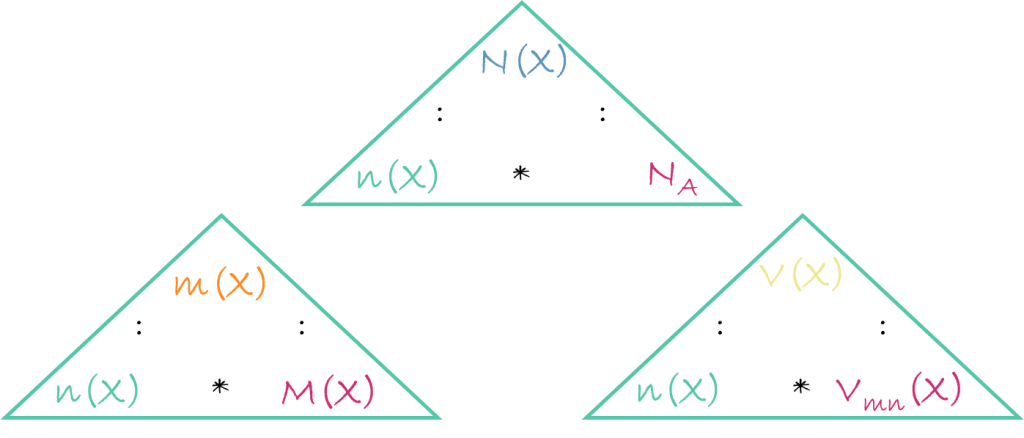
Was ist das Umformungs-Dreieck
Das Umformungs‑Dreieck ist eine grafische Merkhilfe, mit der du Formeln ohne komplizierte Rechenschritte richtig umstellen kannst.
Es besteht aus drei Feldern:
- oben steht die Variable, die alleine im Zähler steht
- unten links und unten rechts stehen die beiden Größen, die du in der Formel im Nenner findest
Das Dreieck zeigt dir sofort, wenn du eine Variable zudeckst:
- Zudecken = Ausrechnen der zugedeckten Variable
Wenn du eine Größe suchst, „deckst“ du sie im Dreieck zu.
Die übrigen Felder zeigen dir automatisch die richtige Rechenoperation.
Beispiele:
- Du suchst die Formel, um V(X) zu berechnen. Dafür deckst du im Dreieck V(X) ab, wodurch im Dreieck nur noch n(X) * Vmn(X) übrig bleibt. Damit kannst du also V(X) berechnen.
- Du möchtest die Stoffmenge n(X) mithilfe der Teilchenzahl N(X) berechnen. Decke also die Stoffmenge n(X) ab. Übrig bleibt im Dreieck N(X) : NA, was deiner Formel zum Berechnen von n(X) entspricht.
Gerade beim Rechnen in der Chemie in der 8. Klasse ist es wichtig, dass Lernende ein Werkzeug an die Hand bekommen, das sie in allen Themenbereichen anwenden können. Das Umformungs‑Dreieck ist genau ein solches Werkzeug: universell einsetzbar, leicht zu verstehen und sofort praktisch nutzbar. Wer es einmal verinnerlicht hat, kann nahezu jede Formel der Mittelstufen‑Chemie problemlos anwenden und umstellen.
Fragen zum Video:
Nach den Grundlagen seid ihr jetzt für die kommenden Übungen gut gerüstet!
Übungen Quantitative Chemie – Rechnen Chemie:
Lösungsvideos:
Übung 03.05.2020: Berechnung Haber-Bosch
Bei der Reaktion von 100 g Stickstoff und der entsprechenden Menge an Wasserstoff entsteht beim Haber-Bosch Verfahren Ammoniak (NH3). Berechne, wie viel Gramm Ammoniak entstehen.
Übung 03.05.2020: Kaliumnitrat wird zu Kaliumnitrit
Übung 03.05.2020: Oxidation von Eisen
Wenn man Eisen der Umwelt aussetzt, dann entsteht bei der Reaktion mit Sauerstoff Eisen(III)-oxid, was auch als Rost bezeichnet wird. Berechne, wie viele Sauerstoffatome zur Bildung von 1 kg Eisen(III)-oxid notwendig sind.


